Detta white paper tillhandahåller kunskap om spektrofotometerkalibrering baserat på kraven i farmakopéerna.
 |
Detta white paper tillhandahåller kunskap om spektrofotometerkalibrering baserat på kraven i farmakopéerna. |
Pharmacopeias är tillsynsmyndigheter som definierar riktlinjer för procedurerna och analysinstrumenten för förberedelse och analytisk mätning av läkemedelsprodukter. Både USA:s farmakopé (USP) och den europeiska farmakopén (Ph. Eur.) har dedikerat kapitel i deras respektive farmakopéer avseende kraven på UV Vis-spektrofotometrar och verifieringen av deras prestanda, nämligen kalibrering av spektrofotometrar. För att säkerställa att kunderna är kompatibla med ändringarna i båda farmakopéerna, som redan implementerades 2020, har METTLER TOLEDO anpassat sina automatiserade prestandaverifieringstillbehör. Detta white paper tillhandahåller en översikt över de viktiga UV Vis-spektroskopirelevanta ändringarna i både USP och Ph. Eur., och tittar närmare på deras inverkan och tillgängliga lösningar för att garantera efterlevnad av regelverk.
Varför är det viktigt med UV Vis-spektrofotometerkalibrering?
Det är viktigt eftersom instrumentprestandan direkt påverkar mätnoggrannheten och repeterbarheten. För kritiska UV Vis-mätningar, i synnerhet inom klinisk eller industriell kvalitetskontroll, är det absolut nödvändigt att instrumentet presterar enligt specifikationerna. I laboratorier som arbetar i enlighet med pharmacopeias regelverk (t.ex. USP eller Ph. Eur.), bör instrumentprestandan övervakas regelbundet och dokumenteras i enlighet med detta.
Vad betyder operativ kvalificering (OQ) för spektrofotometrar?
OQ för spektrofotometrar består vanligtvis av följande tester som krävs av USP och Ph. Eur.:
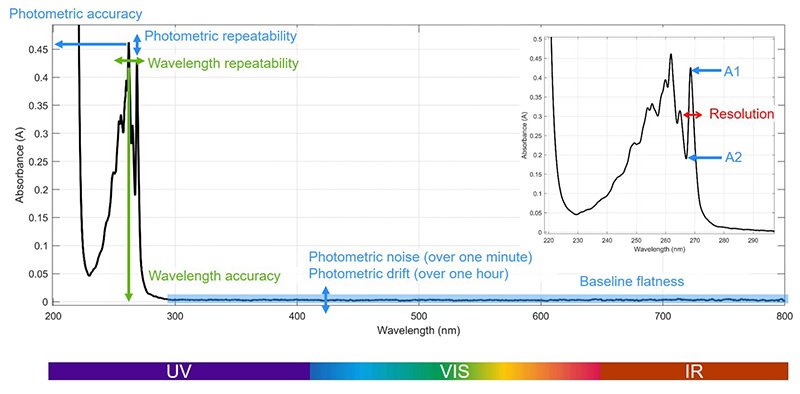
Fotometrisk noggrannhet och repeterbarhet, fotometrisk linjäritet, ströljus, våglängdsnoggrannhet och repeterbarhet, upplösning
Ladda ner detta white paper för information om respektive parametrar och besök kalibrering av UV Vis-spektrofotometer för att ta reda på hur de bestäms i praktiken.
Vad har reviderats från de tidigare versionerna till de senaste versionerna av den europeiska farmakopén och USA:s farmakopé?
Den 1 januari 2020 blev följande ändringar inom operativ kvalificering obligatoriska:
- Bestämningen av fotometrisk linjäritet blev obligatoriskt i båda farmakopéerna.
- I den senaste upplagan av USP, godkänns ströljustest enligt procedur B, vilket är den specifika våglängdsmetoden, förutom procedur A, metoden för lösningsfilterförhållande. Båda metoderna förklaras i kapitel 2.3.4.
- I de nyaste upplagorna av båda farmakopéerna, tillåts användningen av nikotinsyra (Niacin), för fotometrisk kvalificering i UV-regionen, utöver det hittills använda kaliumdikromatet (PDC).
- Båda farmakopéerna kräver kvalificering av samma optiska parametrar. Det enda undantaget är testet på fotometrisk repeterbarhet, vilket krävs av USP.