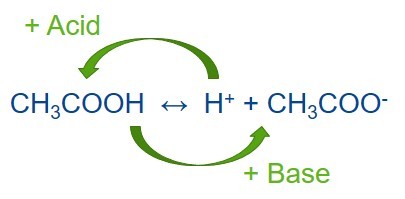
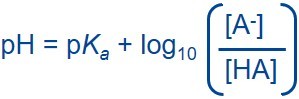A preparação do buffer é um processo comum em laboratórios de química e bioquímica. Uma solução-tampão é uma mistura de um ácido fraco com sua base conjugada ou de uma base fraca com seu ácido conjugado. As soluções-tampão são usadas para ajudar a manter um valor de pH estável de outra solução misturada com o buffer. O buffer resiste a alterações no valor de pH de toda a solução quando uma pequena quantidade de um ácido ou base diferente é introduzida na solução, seja através de adição ou através de qualquer reação química dentro da solução. As soluções-tampão são, portanto, muito úteis em uma grande variedade de aplicações em que é necessário um pH relativamente estável. Um buffer também pode ser denominado buffer de pH, buffer de íons de hidrogênio ou solução-tampão.
Por exemplo, o sangue contém buffers naturais para manter um pH estável entre 7,35 e 7,45, para que as nossas enzimas funcionem corretamente. Como a atividade enzimática varia com o pH, manter um pH constante é essencial em ensaios bioquímicos para garantir o nível correto de atividade. Em aplicações comerciais, os buffers podem ser encontrados nos xampus para evitar a irritação da pele, em loções para bebês para inibir o crescimento de bactérias e em soluções de lentes de contato para garantir que o nível de pH do fluido permaneça compatível com o dos olhos.
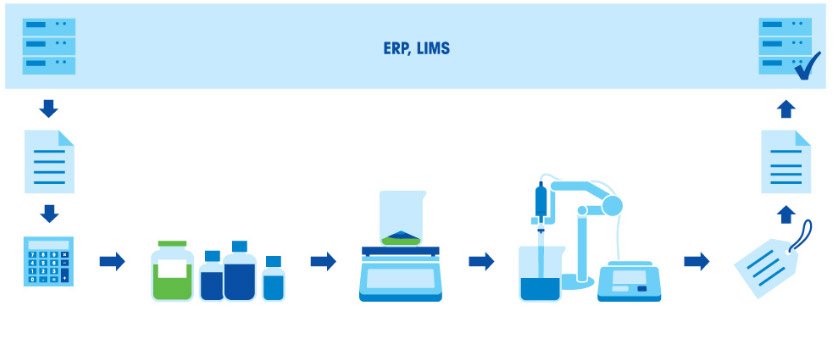
A preparação dos buffers consiste em vários passos: pesagem dos componentes, dissolução dos componentes, ajuste do pH e reposição ao volume final. Uma vez que a relação entre o ácido e a base em um buffer está diretamente relacionada com o pH final, é vital pesar os componentes com um elevado grau de precisão. Assim, é importante que o equipamento utilizado (balança, pipetas e medidor de pH) esteja devidamente calibrado e tenha uma precisão suficiente.