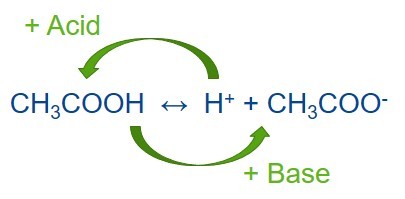
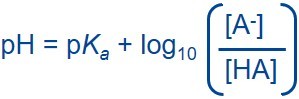Préparer une solution tampon est un processus courant dans les laboratoires de chimie et de biochimie. Une solution tampon est un mélange d'acide faible et de sa base conjuguée ou d'une base faible et de son acide conjugué. On utilise des solutions tampons pour maintenir stable la valeur du pH d'une autre solution mélangée avec le tampon. Le tampon résiste aux variations de la valeur du pH de la totalité de la solution lors de l'introduction d'une petite quantité d'un acide ou d'un alcalin différent dans la solution, soit par ajout, soit par n'importe quelle réaction chimique dans la solution. Les solutions tampons sont donc très utiles dans une gamme étendue d'applications qui exigent un pH relativement stable. Un tampon peut également être appelé tampon pH, tampon aux ions hydronium ou solution tampon.
Ainsi, le sang contient des tampons naturels pour maintenir un pH stable, compris entre 7,35 et 7,45 pour que nos enzymes fonctionnent correctement. Comme l'activité des enzymes varie en fonction du pH, le maintien d'un pH constant est essentiel dans les analyses biochimiques afin de garantir un niveau correct d'activité. Dans les applications commerciales, on trouve des tampons dans les shampoings pour empêcher les irritations cutanées, dans les lotions pour bébés pour empêcher la prolifération de bactéries et dans les solutions pour lentilles de contact pour garantir que le pH du fluide reste compatible avec celui de l'œil.
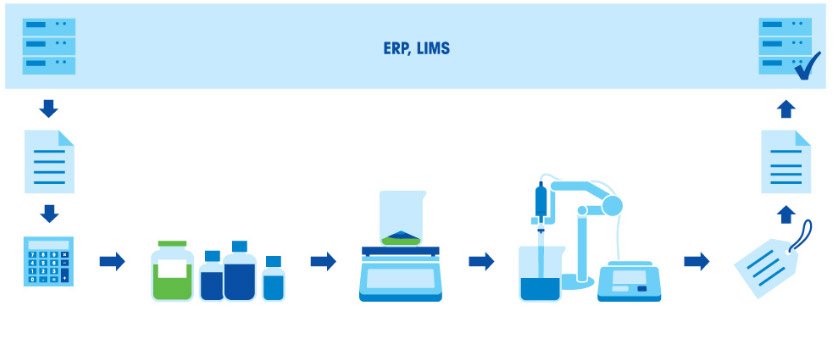
Préparer une solution tampon comporte plusieurs étapes : le pesage des composants, la dissolution des composants, l'ajustement du pH et le renouvellement au volume final. Comme le rapport acide/base dans un tampon est directement fonction du pH final, il est essentiel de procéder au pesage des composants avec un excellent degré de précision. Il est donc important que les équipements utilisés (balance, pipettes et pH-mètre) soient correctement calibrés et suffisamment précis.