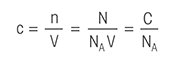Poniższe definicje miareczkowania mogą ułatwić Państwu naukę wszystkiego, co trzeba wiedzieć o miareczkowaniu.
Analit: Określona substancja chemiczna w próbce, której zawartość lub ilość jest określana przez miareczkowanie.
Koniec miareczkowania: Pożądany punkt końcowy lub punkt równoważności, w którym miareczkowanie zostaje zakończone, a zużycie titranta ocenione. Podczas tego samego miareczkowania może wystąpić więcej niż jeden punkt równoważnikowy.
Punkt końcowy: Punkt, w którym obserwowany jest koniec reakcji miareczkowania (zazwyczaj poprzez zmianę koloru lub inny wskaźnik miareczkowania). Zdefiniowanie miareczkowania wraz z jego punktem końcowym stanowi klasyczną technikę.
Punkt równoważności: Punkt, w którym liczba jednostek (równoważników) dodanego titranta jest taka sama jak liczba jednostek analitu próbki.
Wskazanie: Procedura śledzenia reakcji i wykrywania końca miareczkowania. Ogólnie rzecz biorąc, wskazanie odbywa się za pomocą potencjometrii (elektrod) lub kolorowych wskaźników.
Paralaksa: Różnica w pozornym położeniu obiektu w oparciu o linię wzroku obserwatora. W miareczkowaniu zjawisko to należy uwzględnić podczas wizualnej obserwacji menisku cieczy w biurecie.
Wzorzec pierwotny: Certyfikowana, wysoce czysta substancja używana do dokładnego określania stężenia titranta.
Akwizycja sygnału: Akwizycja sygnału to monitorowanie zjawisk fizycznych w celu uzyskania wartości cyfrowych lub liczbowych w określonych punktach (takich jak punkt końcowy eksperymentu miareczkowania lub punkt równoważności).
Standaryzacja: Wykorzystanie wysoce czystej referencyjnej substancji chemicznej (wzorca) do określenia stężenia titranta.
Stechiometria: Zależności mol/masa między odczynnikami i produktami w miareczkowaniu. Odczynniki miareczkujące reagują zgodnie z ustalonymi zależnościami, więc jeśli znana jest ilość poszczególnych reagentów, można obliczyć ilość produktu. Jeśli znana jest ilość jednego reagenta i można określić ilość produktów, można również obliczyć ilość innych reagentów.
Titrant: Roztwór określonego odczynnika chemicznego, który jest znormalizowany pod względem stężenia, dzięki czemu może być używany do dokładnego miareczkowania.
Miareczkowanie: Ilościowa analiza chemiczna, w której określona ilość titranta reaguje ilościowo z analizowanym związkiem próbki. Na podstawie objętości zużytego titranta oblicza się ilość związku próbki w oparciu o stechiometrię reakcji testowej. Znana również jako wolumetria lub miareczkowanie.
Krzywa miareczkowania: Krzywe miareczkowania ilustrują jakościowy postęp miareczkowania. Krzywa zazwyczaj wykorzystuje objętość titranta jako zmienną niezależną, a roztwór jako zmienną zależną. Krzywa umożliwia szybką ocenę metody miareczkowania. Krzywe przyjmują cztery formy: symetryczną, asymetryczną, minimum/maksimum i segmentową.
Cykl miareczkowania: Cykl, który jest wykonywany i powtarzany do momentu osiągnięcia punktu końcowego lub punktu równoważności reakcji miareczkowania. Cykl miareczkowania składa się głównie z czterech etapów: dodawania titranta, reakcji miareczkowania, pozyskiwania sygnału i oceny.
Równanie miareczkowania: Seria wzorów miareczkowania, które umożliwiają obliczenie masowej molarności próbek stałych, stężenia roztworów kwasów i zasad, stężenia rozcieńczonych roztworów oraz zużycia titranta po bezpośrednim miareczkowaniu. Aby łatwo obliczyć wyniki miareczkowania, prosimy odwiedzić nasz Kalkulator miareczkowania.
Teoria miareczkowania: Teoria miareczkowania bada oznaczanie produktu w zależności od jego stężenia poprzez obserwację reakcji miareczkowania przy użyciu metod fizycznych lub elektrochemicznych. Znajomość dokładnego stężenia gatunku, produktu lub funkcji chemicznej pomaga zapewnić wydajność procesu i/lub jakość produktu.