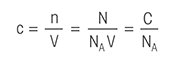Aşağıdaki titrasyon tanımları, titrasyon hakkında bilmeniz gereken her şeyi öğrenmenizi kolaylaştırabilir.
Analit: İçeriği veya miktarı titrasyonla belirlenen bir numunedeki spesifik kimyasal türler.
Titrasyon sonu: Titrasyonun sonlandırıldığı ve titrant tüketiminin değerlendirildiği istenen son nokta veya eşdeğerlik noktası. Aynı titrasyon sırasında birden fazla eşdeğerlik noktası oluşabilir.
Bitiş Noktası: Titrasyon reaksiyonunun sonunun gözlendiği nokta (tipik olarak renk değişimi veya başka bir titrasyon göstergesi ile). Titrasyonu bitiş noktası ile birlikte tanımlamak klasik tekniği temsil eder.
Eşdeğerlik noktası: Eklenen titrantın varlık sayısının (eşdeğer) numune analitinin varlık sayısı ile aynı olduğu nokta.
İndikasyon: Reaksiyonu takip etmek ve titrasyonun sonunu tespit etmek için kullanılan prosedür. Genel olarak indikasyon potansiyometri (elektrotlar) veya renk indikatörleri kullanılarak yapılır.
Paralaks: Gözlemcinin görüş hattına bağlı olarak bir nesnenin görünen konumundaki fark. Titrasyonda, bir büret içindeki sıvı menisküsleri görsel olarak gözlemlerken bu fenomen göz önünde bulundurulmalıdır.
Birincil standart: Titrant konsantrasyonunun doğru şekilde belirlenmesi için kullanılan sertifikalı, yüksek saflıkta bir madde.
Sinyal toplama: Sinyal alımı, belirli noktalarda (titrasyon deneyi bitiş noktası veya eşdeğerlik noktası gibi) dijital veya sayısal değerler elde etmek için fiziksel olayların izlenmesidir.
Standardizasyon: Titrant konsantrasyonunu belirlemek için oldukça saf bir referans kimyasal maddenin (standart) kullanılması.
Stokiyometri: Titrasyonda reaktifler ve ürünler arasındaki mol/kütle ilişkileri. Titrasyon reaktifleri sabit ilişkilere göre reaksiyona girer, bu nedenle ayrı reaktanların miktarı biliniyorsa, ürünün miktarı hesaplanabilir. Bir reaktantın miktarı biliniyorsa ve ürünlerin miktarı belirlenebiliyorsa, diğer reaktantların miktarı da hesaplanabilir.
Titrant: Doğru titrasyon için kullanılabilmesi için konsantrasyon açısından standardize edilmiş belirli bir kimyasal reaktif çözeltisi.
Titrasyon: Belirli bir miktarda titrantın analiz edilen örnek bileşikle nicel olarak reaksiyona girdiği nicel bir kimyasal analiz. Tüketilen titrant hacminden, numune bileşiğinin miktarı tahlil reaksiyonunun stokiyometrisine dayalı olarak hesaplanır. Volumetri veya titrimetri olarak da bilinir.
Titrasyon eğrisi: Titrasyon eğrileri bir titrasyonun niteliksel ilerleyişini gösterir. Eğri genellikle bağımsız değişken olarak titrant hacmini ve bağımlı değişken olarak çözeltiyi kullanır. Eğri, titrasyon yönteminin hızlı bir şekilde değerlendirilmesini sağlar. Eğriler dört şekilde olabilir: simetrik, asimetrik, minimum/maksimum ve parçalı.
Titrasyon döngüsü: Titrasyon reaksiyonunun bitiş noktasına veya eşdeğerlik noktasına ulaşılana kadar gerçekleştirilen ve tekrarlanan döngü. Titrasyon döngüsü temel olarak dört adımdan oluşur: titrant ekleme, titrasyon reaksiyonu, sinyal alma ve değerlendirme.
Titrasyon denklemi: Katı numunelerin kütle molaritesinin, asit ve baz çözeltilerinin konsantrasyonunun, seyreltilmiş çözeltilerin konsantrasyonunun ve doğrudan titrasyondan sonra titrant tüketiminin hesaplanmasını sağlayan bir dizi titrasyon formülü. Titrasyon sonuçlarını kolayca hesaplamak için Titrasyon Hesaplayıcımızı ziyaret edin.
Titrasyon teorisi: Titrasyon teorisi, fiziksel veya elektrokimyasal yöntemler kullanarak bir titrasyon reaksiyonunu gözlemleyerek konsantrasyonuyla ilgili bir ürünün belirlenmesini araştırır. Bir türün, ürünün veya kimyasal fonksiyonun tam konsantrasyonunun bilinmesi, proses verimliliğinin ve/veya ürün kalitesinin sağlanmasına yardımcı olur.