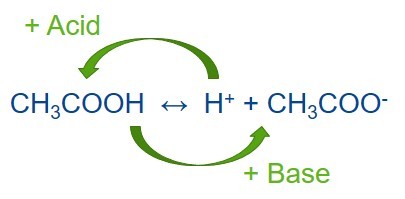
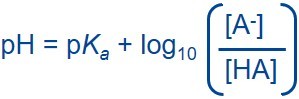Przygotowanie buforu to często spotykany proces w laboratoriach chemicznych i biochemicznych. Roztwór buforowy stanowi mieszaninę słabego kwasu i jego sprzężonej zasady albo słabej zasady i jej sprzężonego kwasu. Roztwory buforowe stosuje się w celu utrzymania stabilnej wartości pH innego roztworu mieszanego z buforem. Bufor jest odporny na zmiany wartości pH całego roztworu, gdy niewielka ilość innego kwasu lub zasady zostanie wprowadzona do roztworu przez dodanie lub w wyniku dowolnej reakcji chemicznej wewnątrz roztworu. Roztwory buforowe są zatem bardzo przydatne w wielu różnych zastosowaniach wymagających stosunkowo stabilnego pH. Bufor może być również nazywany buforem pH, buforem jonów wodorowych lub roztworem buforowym.
Na przykład krew zawiera naturalne bufory utrzymujące stabilną wartość pH między 7,35 a 7,45, dzięki czemu nasze enzymy działają prawidłowo. Ponieważ aktywność enzymów zmienia się w zależności od pH, utrzymanie jego stałego poziomu jest niezbędne w testach biochemicznych w celu zapewnienia prawidłowego poziomu aktywności. W zastosowaniach komercyjnych bufory występują w szamponach zapobiegających podrażnieniom skóry, balsamach dla niemowląt hamujących wzrost bakterii oraz roztworach do soczewek kontaktowych zapewniających utrzymanie poziomu pH płynu odpowiadającego poziomowi pH oka.
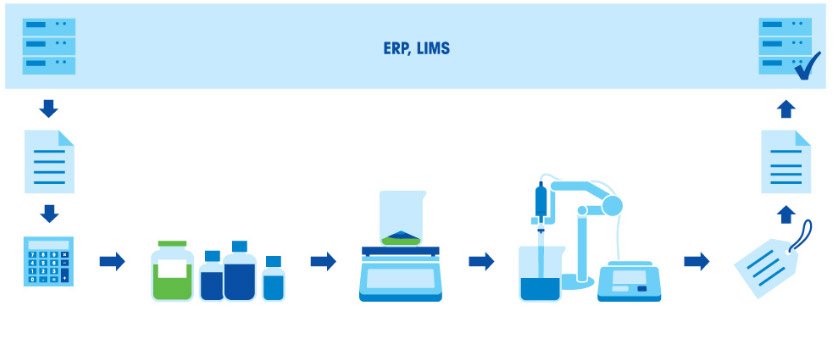
Przygotowanie buforów obejmuje kilka etapów: odważanie składników, rozpuszczenie składników, dostosowanie pH i uzupełnienie do końcowej objętości. Ponieważ proporcja kwasu do zasady w buforze jest bezpośrednio związana z końcowym pH, składniki należy ważyć z dużą dokładnością. Niezwykle istotne jest zatem, by używany sprzęt (waga, pipety i miernik pH) był właściwie wzorcowane i miały odpowiednią dokładność.