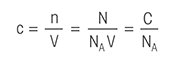Følgende titreringsdefinitioner kan gøre det lettere for dig at lære alt, hvad du behøver at vide om titrering.
Analyt: Specifik kemisk art i en prøve, hvis indhold eller mængde bestemmes ved titrering.
Slut på titreringen: Det ønskede slutpunkt eller ækvivalenspunkt, hvor titreringen afsluttes, og forbruget af titreringsmiddel evalueres. Der kan forekomme mere end ét ækvivalenspunkt under den samme titrering.
Slutpunkt: Det punkt, hvor afslutningen af titreringsreaktionen observeres (typisk ved farveændring eller en anden titreringsindikator). At definere en titrering sammen med dens endepunkt er den klassiske teknik.
Ækvivalenspunkt: Det punkt, hvor antallet af enheder (ækvivalenter) af det tilsatte titreringsmiddel er det samme som antallet af enheder af prøveanalytten.
Indikation: Proceduren til at følge reaktionen og detektere afslutningen af titreringen. Generelt foretages indikation ved hjælp af potentiometri (elektroder) eller farveindikatorer.
Parallakse: Forskellen i den tilsyneladende position af et objekt baseret på observatørens synslinje. Ved titrering skal dette fænomen tages i betragtning, når man visuelt observerer flydende menisker i en burette.
Primær standard: Et certificeret, meget rent stof, der bruges til nøjagtig bestemmelse af titrantkoncentrationen.
Signalopsamling: Signalopsamling er overvågning af fysiske fænomener for at opnå digitale eller numeriske værdier på bestemte punkter (f.eks. et titreringseksperiments slutpunkt eller ækvivalenspunkt).
Standardisering: Brug af et meget rent kemisk referencestof (standard) til at bestemme koncentrationen af titreringsmiddel.
Støkiometri: Mol/masse-forhold mellem reagenser og produkter i en titrering. Titreringsreagenser reagerer i henhold til faste forhold, så hvis mængden af separate reaktanter er kendt, kan mængden af produktet beregnes. Hvis mængden af en reaktant er kendt, og mængden af produkter kan bestemmes, kan mængden af andre reaktanter også beregnes.
Titrant: En opløsning af et bestemt kemisk reagens, der er standardiseret med hensyn til koncentration, så det kan bruges til nøjagtig titrering.
Titrering: En kvantitativ kemisk analyse, hvor en defineret mængde titreringsmiddel reagerer kvantitativt med den prøveforbindelse, der analyseres. Ud fra den mængde titreringsmiddel, der forbruges, beregnes mængden af prøveforbindelse baseret på støkiometrien for assayreaktionen. Også kendt som volumetri eller titrimetri.
Titreringskurve: Titreringskurver illustrerer det kvalitative forløb af en titrering. Kurven bruger generelt volumenet af titreringsmidlet som den uafhængige variabel og opløsningen som den afhængige variabel. En kurve giver mulighed for hurtig vurdering af titreringsmetoden. Kurver har fire former: symmetrisk, asymmetrisk, minimum/maximum og segmenteret.
Titreringscyklus: Den cyklus, der udføres og gentages, indtil slutpunktet eller ækvivalenspunktet for titreringsreaktionen er nået. Titreringscyklussen består primært af fire trin: tilsætning af titreringsmiddel, titreringsreaktion, signalopsamling og evaluering.
Titreringsligning: En række titreringsformler, der gør det muligt at beregne massemolariteten af faste prøver, koncentrationen af syre- og baseopløsninger, koncentrationen af fortyndede opløsninger og forbruget af titreringsmiddel efter en direkte titrering. For nem beregning af titreringsresultater, besøg vores Titration Calculator.
Titreringsteori: Titreringsteori udforsker bestemmelsen af et produkt relateret til dets koncentration ved at observere en titreringsreaktion ved hjælp af enten fysiske eller elektrokemiske metoder. At kende den nøjagtige koncentration af en art, et produkt eller en kemisk funktion er med til at sikre proceseffektivitet og/eller produktkvalitet.